

近日,我系李丹教授课题组在Environmental Science & Technology上发表题为“Nanoplastics in Simulated Human Lung Fluids: Aggregation Kinetics, Theoretical Model Simulation, and Effects on Pulmonary Bacteria”的研究论文,并被选为内封面文章(supplementary cover)。呼吸吸入是人体暴露纳米塑料的重要途径之一,然而其在肺部复杂微环境中的行为及潜在毒性仍缺乏系统研究。本研究通过模拟健康与炎症状态下的人体肺液,系统探讨了不同粒径与表面修饰的聚苯乙烯纳米塑料(PSNPs)的凝聚行为、相互作用机制,以及对肺部原生与致病菌的毒性效应。结果表明,PSNPs在炎症人工溶酶体液(artificial lysosomal fluid, ALF)中均发生凝聚,而未表面修饰和羧基修饰的PSNPs在健康的Gamble溶液(Gamble’s solution, GS)和添加肺表面活性剂的Gamble溶液(modified GS, MGS)中保持稳定。冗余分析表明,PSNPs的凝聚减轻了其对细菌的氧化应激和膜损伤。氨基修饰的PSNPs在GS中可诱导持续的氧化应激,损伤细菌的细胞膜,并促使致病铜绿假单胞菌释放绿脓菌素升高至对照组的2.16倍。此外,塑料老化过程显著增强了PSNPs对肺部细菌的毒性。本研究为纳米塑料在肺部中的行为和毒性作用提供了新见解。

纳米塑料的普遍存在对全球公共健康构成了严重威胁,其中呼吸吸入被认为是人体暴露的主要途径,已有研究证实其可进入人体肺部。纳米塑料在肺部中的凝聚会影响其暴露剂量和毒性特征,深入了解其在肺液中的凝聚行为与相互作用对评估其毒性和健康危害至关重要。另外,肺部微生物群在维持肺部稳态方面发挥关键作用,而肺部微环境如何调控纳米塑料与微生物群相互作用的机制尚不清楚。
本研究通过三种模拟肺液(代表健康与炎症状态),结合DLVO理论与表征实验,深入揭示了纳米塑料的凝聚机制及肺表面活性剂的调控效应。进一步探讨了纳米塑料对肺部原生细菌和机会性致病菌的毒性作用和潜在机制,建立了纳米塑料凝聚行为与生物毒性之间的关联。
PSNPs在模拟人体肺液中的凝聚动力学
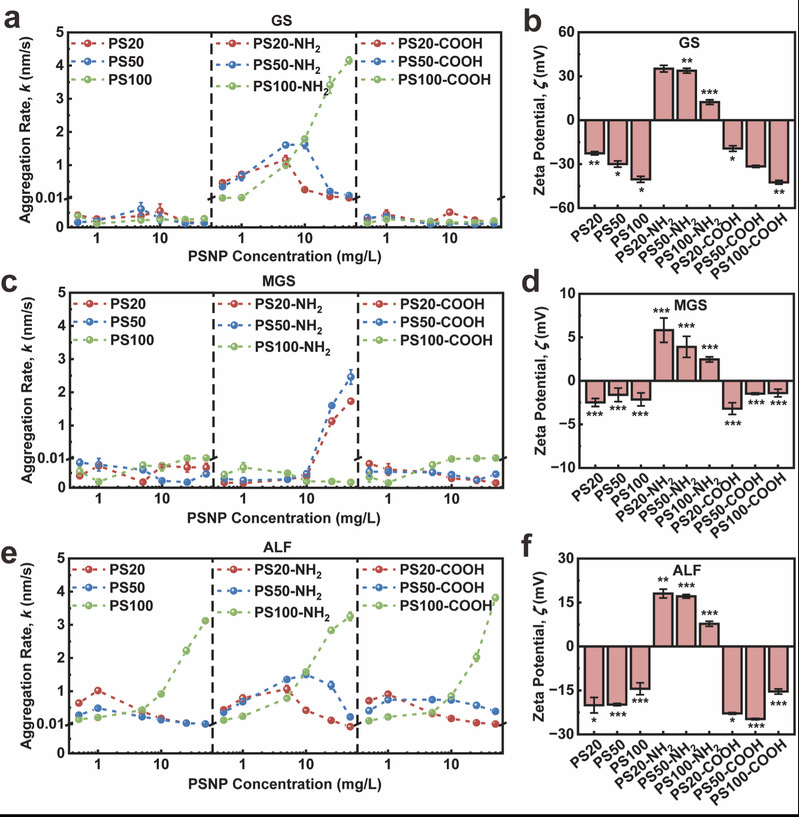
图1:纳米塑料在不同肺液中的胶体稳定性:PSNPs在(a)GS,(c)MGS和(e)ALF中的凝聚速率;PSNPs在(b)GS,(d)MGS和(f)ALF中的ζ电位。
在GS中,PS和PS-COOH保持稳定,而PS-NH2由于电荷中和作用导致ζ电位显著减弱,出现明显凝聚。在含有肺表面活性剂的MGS中,仅高浓度PS20-NH2和PS50-NH2发生凝聚,所有PSNPs的ζ电位绝对值均低于6 mV,表明肺表面活性剂在调控PSNPs凝聚行为中发挥关键作用。在ALF中,九种PSNPs均表现出不同程度的凝聚。
肺液组分对PSNPs凝聚的影响
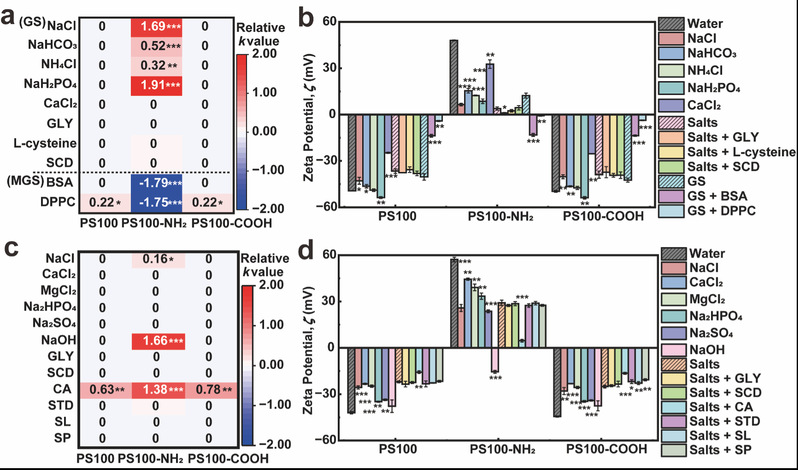
图2:肺液组分对纳米塑料胶体稳定性的影响:(a)GS/MGS,(c)ALF组分存在下PSNPs的相对凝聚速率;(b)GS/MGS,(d)ALF组分对PSNPs ζ电位的影响。
基于PSNPs在肺液中的不同凝聚行为,系统评估了肺液组分对PSNPs凝聚行为的影响。结果表明,GS中的无机组分(NaCl、NaHCO3、NH4Cl和NaH2PO4)通过压缩双电层效应,显著提高PS100-NH2的凝聚速率。而肺表面活性剂(BSA和DPPC)则有效吸附在PSNPs表面,分别通过空间位阻效应与自组装胶束结构,显著增强PS100-NH2的胶体稳定性。此外,ALF中的柠檬酸是调控PSNPs凝聚行为的关键组分。
基于DLVO理论预测PSNPs的凝聚行为
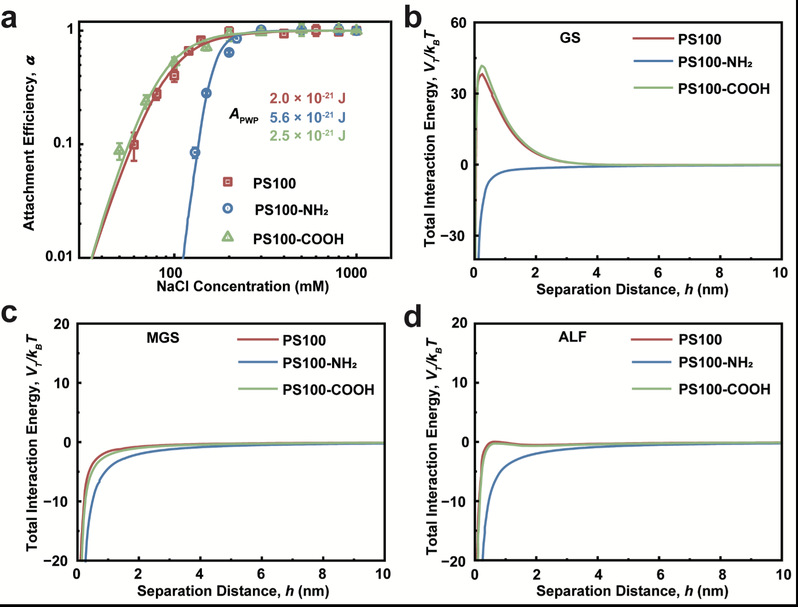
图3:基于DLVO理论的PSNPs凝聚行为预测:(a)PSNPs在NaCl溶液中的实验附着效率DLVO拟合;DLVO理论计算PSNPs在(b)GS, (c)MGS和(d)ALF中的总相互作用能。
PSNPs在GS和ALF中的凝聚行为遵循经典DLVO理论,主要受范德华力和静电斥力的共同调控;而在MGS中,非DLVO作用力起主导作用,推测PSNPs的稳定性增强是由于肺表面活性剂吸附在颗粒表面产生的空间位阻效应。
PSNPs与肺表面活性剂的相互作用机制
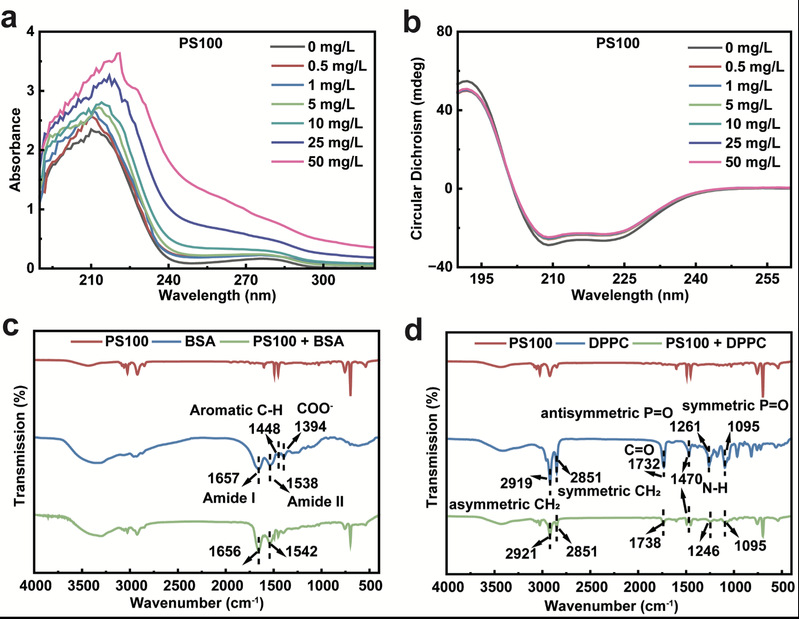
图4:PSNPs与肺表面活性剂的相互作用机制:BSA与不同浓度PS100相互作用的(a)UV-vis光谱和(b)圆二色光谱;(c)PS100、BSA以及BSA与PS100作用混合物的FTIR光谱;(d)PS100、DPPC以及DPPC与PS100作用混合物的FTIR光谱。
通过表征实验系统研究了PSNPs与肺表面活性剂之间的相互作用机制。UV-vis光谱结果显示,与PSNPs相互作用后,BSA特征峰强度增强并发生红移,表明PSNPs扰乱了BSA微环境并诱导其发生构象变化。圆二色光谱进一步揭示PSNPs导致BSA二级结构的破坏。FTIR结果表明,PSNPs与BSA多肽中的C=O、C–N或N–H基团相互作用,从而诱导蛋白质二级结构发生变化。此外,PSNPs通过氢键与DPPC双分子层中的羰基和酰胺基团结合,破坏DPPC头部基团,进而导致脂质双层的不稳定性。
PSNPs在不同肺液中对肺部原生细菌和机会性致病菌的影响
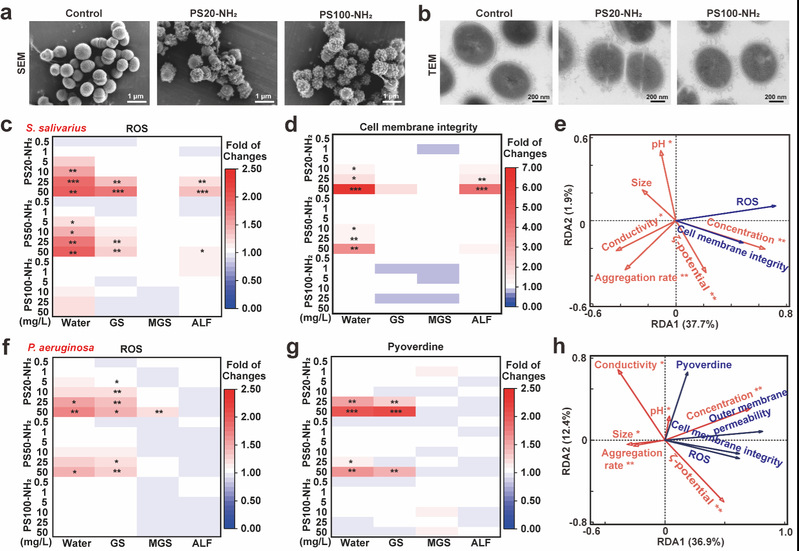
图5:PSNPs对肺部原生细菌和机会性致病菌的影响:PSNPs处理前后唾液链球菌的(a)SEM和(b)TEM图像;PS-NH2在不同环境(Water,GS,MGS和ALF)中对唾液链球菌(c)ROS生成和(d)细胞膜完整性的影响;(e)环境变量(ζ电位、凝聚速率、粒径、浓度、pH值和电导率)与唾液链球菌反应(ROS和细胞膜完整性)之间的冗余分析;PS-NH2在不同环境(Water,GS,MGS和ALF)中对铜绿假单胞菌(f)ROS生成和(g)绿脓菌素生成的影响;(h)环境变量(ζ电位、凝聚速率、粒径、浓度、pH值和电导率)与铜绿假单胞菌反应(ROS、细胞膜完整性、外膜通透性和绿脓菌素)之间的冗余分析。
唾液链球菌和铜绿假单胞菌分别代表肺部原生细菌和机会性致病菌,用于评估PSNPs在不同肺环境中的生物毒性效应。结果表明,在健康肺液中,PSNPs可诱导持续性氧化应激并有效破坏细胞膜结构;在50 mg/L PS20-NH2处理下,铜绿假单胞菌的绿脓菌素分泌量显著提升至对照组的2.16倍。冗余分析进一步揭示,PSNPs的毒性效应与其凝聚速率呈负相关关系,表明凝聚行为可在一定程度上缓解其对肺部微生物的毒性。
紫外老化对PSNPs毒性的影响
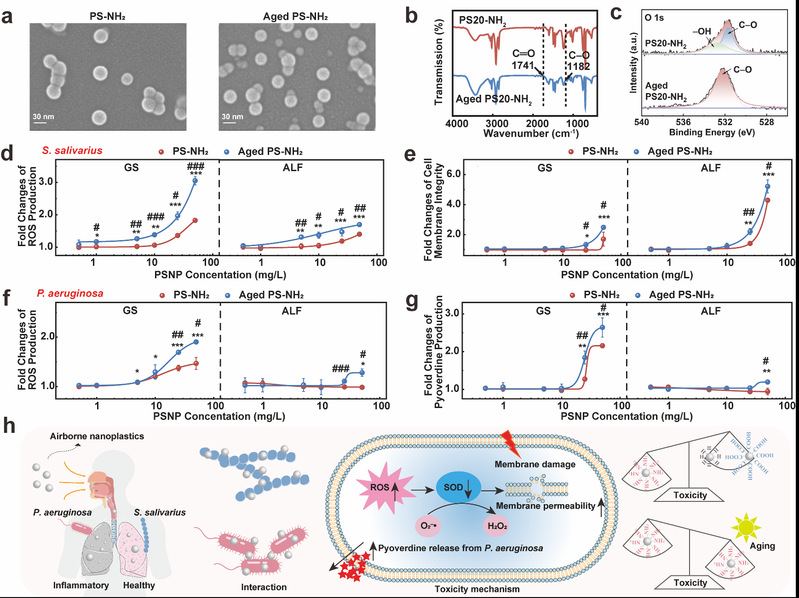
图6:老化PSNPs对肺部原生细菌和机会性致病菌的影响:(a)原始和老化PS-NH2的(a)SEM图像、(b)FTIR光谱和(c)XPS O 1s能谱;原始和老化PS-NH2在GS和ALF中对唾液链球菌(d)ROS生成和(e)细胞膜完整性的影响;原始和老化PS-NH2在GS和ALF中对铜绿假单胞菌(f)ROS生成和(g)绿脓菌素生成的影响;(h)PSNPs对肺部细菌的毒性机制图。
紫外老化处理后,PSNPs表面呈现粗糙化,粒径减小,表面含氧官能团增多。毒性实验结果表明,老化显著增强了PSNPs对肺部细菌的毒性,强调了环境老化过程在评估纳米塑料对人体健康风险中的关键作用。
本研究表明,未修饰和羧基修饰的PSNPs在健康肺液(GS和MGS)中保持稳定,归因于其强表面电位和肺表面活性剂产生的空间位阻效应;在炎症肺液(ALF)中,由于强电荷屏蔽作用,所有PSNPs均表现出不同程度的凝聚。研究强调了颗粒粒径、表面修饰和肺部微环境在胶体行为中的关键作用。毒性结果表明氧化应激是PSNPs重要毒性机制,冗余分析证实PSNPs的凝聚行为减轻了其对肺部的毒性作用。另外,PSNPs在环境中的老化过程显著增强其对肺部细菌的毒性。本研究成果拓展了对纳米塑料行为与毒性的理解,为公共健康风险评估提供理论基础和实验依据。
论文第一作者为我系博士研究生邵志伟,李丹教授为通讯作者,陈建民教授为研究合作者。本研究得到国家重点研发计划、广州国家实验室重大项目、国家自然科学基金以及上海市科学技术委员会的支持。
文章链接:https://pubs.acs.org/doi/10.1021/acs.est.5c06466
供稿:李丹课题组
审核:张立武











